Mirabilit: Unterschied zwischen den Versionen
| Zeile 103: | Zeile 103: | ||
In Anwesenheit von Fremdionen (bei Salzgemischen) verändern sich die Parameter der Gleichgewichtsfeuchte und der notwendigen Temperatur- und Feuchtebedingungen für Umkristallisationen zudem deutlich. Als orientierende Daten sind in Tabelle ?? experimentell erfasste Werte der Gleichgewichtsfeuchte in unterschiedlichen Salzgemischen wiedergegeben. Es zeigt sich, dass alle Werte der Gleichgewichtsfeuchte unter denen des Reinsalzes Mirabilit liegen. | In Anwesenheit von Fremdionen (bei Salzgemischen) verändern sich die Parameter der Gleichgewichtsfeuchte und der notwendigen Temperatur- und Feuchtebedingungen für Umkristallisationen zudem deutlich. Als orientierende Daten sind in Tabelle ?? experimentell erfasste Werte der Gleichgewichtsfeuchte in unterschiedlichen Salzgemischen wiedergegeben. Es zeigt sich, dass alle Werte der Gleichgewichtsfeuchte unter denen des Reinsalzes Mirabilit liegen. | ||
{| cellspacing="1" cellpadding="1" border="1" style="width: | {| cellspacing="1" cellpadding="1" border="1" style="width: 500px; height: 65px;" | ||
|+'''Tabelle 1''': Angaben der Gleichgewichtsfeuchten über gesättigten Mischlösungen (Mischungsverhältnis: Gesättigte Lsg.A/ gesättigte Lsg.B =1:1) <bib id="Vogt.etal:1993"/>.'' | |+'''Tabelle 1''': Angaben der Gleichgewichtsfeuchten über gesättigten Mischlösungen (Mischungsverhältnis: Gesättigte Lsg.A/ gesättigte Lsg.B =1:1) <bib id="Vogt.etal:1993"/>.'' | ||
|- | |- | ||
| Zeile 149: | Zeile 149: | ||
| 15 | | 15 | ||
|} | |} | ||
== Kristallisationsdruck == | == Kristallisationsdruck == | ||
Version vom 30. Juli 2010, 13:26 Uhr
<bibimport/>
| Mirabilit[1][2][3] | |

| |
| Mineralogische Salzbezeichnung | Mirabilit |
| Chemische Bezeichnung | Natriumsulfadecahydrat |
| Trivialname | Glaubersalz, Reussin, Wundersalz |
| Chemische Formel | Na2SO4•10H2O |
| Hydratformen |
Natriumsulfatheptahydrat (Na2SO4•7H2O) |
| Kristallklasse | monoklin |
| Deliqueszenzfeuchte 20°C | 93,6 |
| Dichte (g/cm³) | 1,464 g/cm³ |
| Molvolumen | 219,8 cm3/mol |
| Molgewicht | 322,21 g/mol |
| Transparenz | durchsichtig bis undurchsichtig |
| Spaltbarkeit | vollkommen bis schlecht |
| Kristallhabitus | |
| Zwillingsbildung | |
| Brechungsindices | nx = 1,395 ny = 1,396-1,410 nz = 1,398-1,419 |
| Doppelbrechung | Δ = 0,04-0,023 |
| Optische Orientierung | negativ |
| Pleochroismus | |
| Dispersion | |
| Phasenübergang | |
| Chemisches Verhalten | |
| Bemerkungen | löslich in Wasser und Glycerin, in wasserfreiem Ethanol unlöslich |
Autoren: Hans-Jürgen Schwarz , Nils Mainusch, NN....
zurück zu Sulfate
Abstract[Bearbeiten]
Vorkommen von Mirabilit[Bearbeiten]
siehe Natriumsulfat
Angaben zu Herkunft und Bildung von Mirabilit an Baudenkmalen[Bearbeiten]
siehe Natriumsulfat
Lösungsverhalten[Bearbeiten]
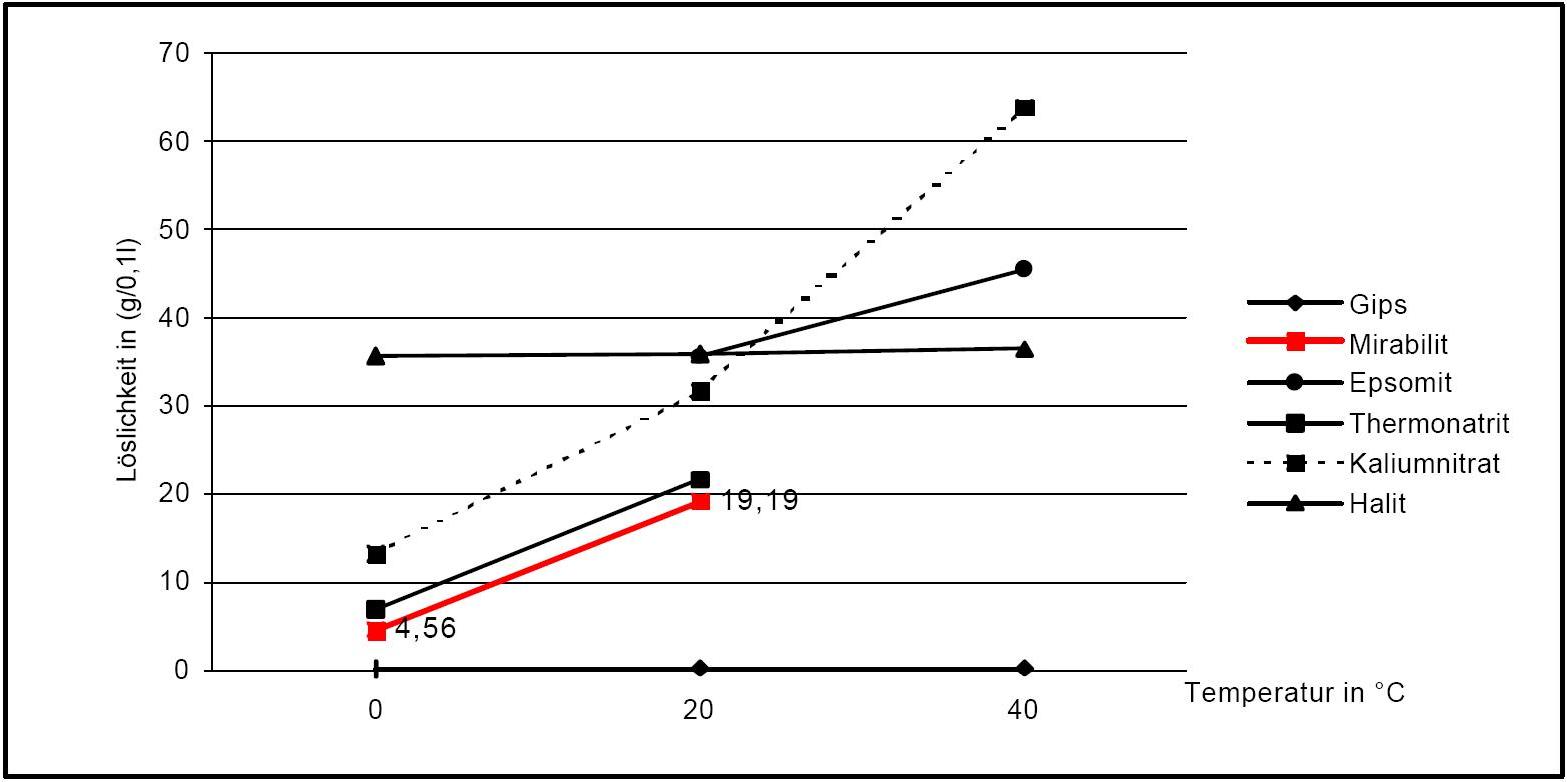
Vergleich mit anderen Salzphasen [Angaben nach [Stark.etal:1996]Titel: Bauschädliche Salze
Autor / Verfasser: Stark, Jochen; Stürmer, Sylvia
 ].
].siehe Natriumsulfat
Hygroskopizität[Bearbeiten]
In Abbildung 1 ist der Temperatureinfluss auf die Deliqueszenzpunkte von Thenardit und Mirabilit verdeutlicht. Auffällig sind hierbei die gegenläufigen Kurvengänge.
In Anwesenheit von Fremdionen (bei Salzgemischen) verändern sich die Parameter der Gleichgewichtsfeuchte und der notwendigen Temperatur- und Feuchtebedingungen für Umkristallisationen zudem deutlich. Als orientierende Daten sind in Tabelle ?? experimentell erfasste Werte der Gleichgewichtsfeuchte in unterschiedlichen Salzgemischen wiedergegeben. Es zeigt sich, dass alle Werte der Gleichgewichtsfeuchte unter denen des Reinsalzes Mirabilit liegen.
| RF % | MgSO4 | Ca(NO3)2 | KNO3 |
| Na2SO4 • 10H2O | 87(21°C) | 74 (21°C) | 81(21°C) |
Feuchtesorption:
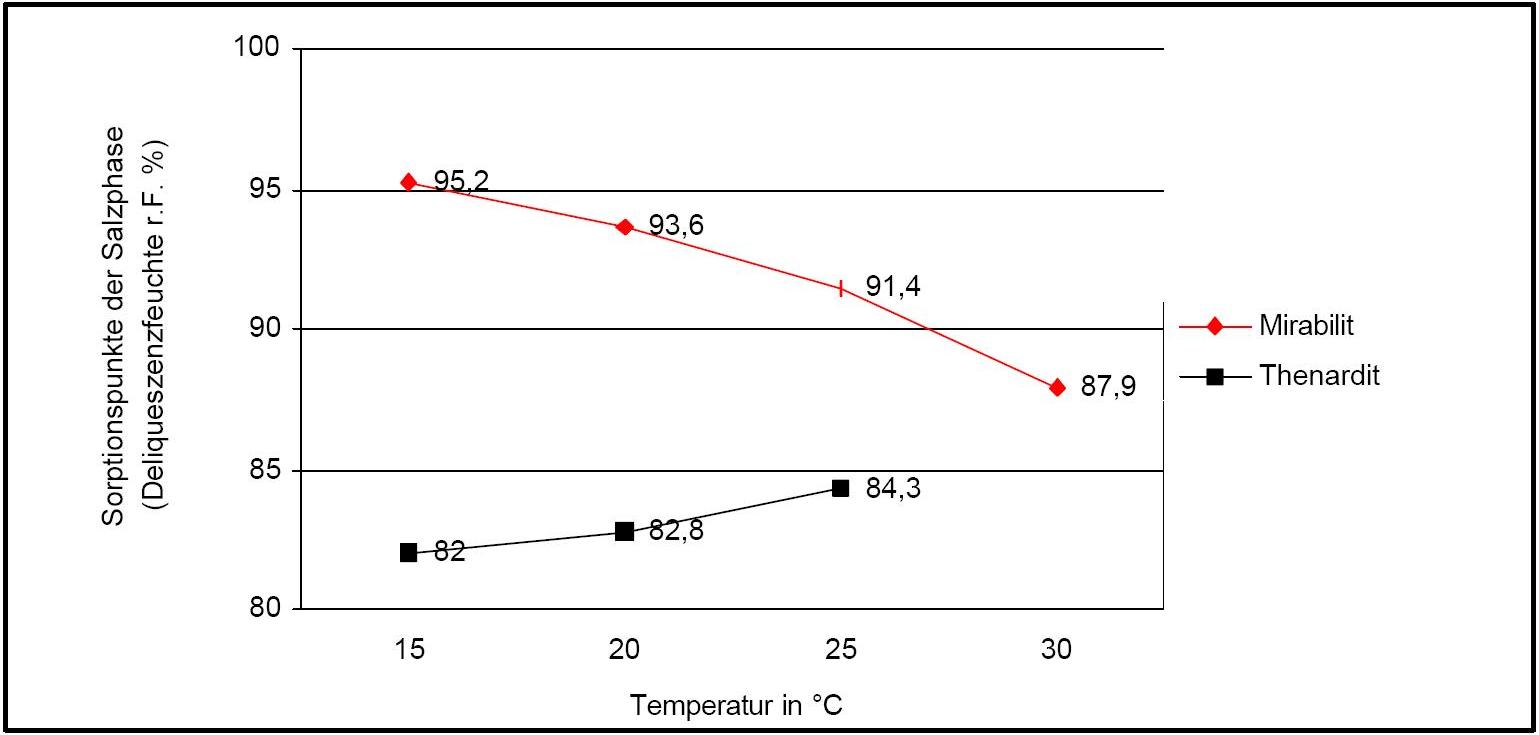
Autor / Verfasser: Arnold, Andreas; Zehnder, Konrad

Als weitere Angabe zur Abschätzung der Hygroskopizität von Natriumsulfaten sind in der nachstehenden Tabelle Werte für das Sorptionsverhalten des Reinsalzes und des Gemisches mit Halit bei unterschiedlichen relativen Feuchten wiedergegeben:
Feuchtsorption in M.% nach 56 Tagen Lagerung bei:
| Feuchtsorption in M.% nach 56 Tagen Lagerung bei | |||
| Lagerungsfeuchte | 87% r.F. | 81% r.F. | 79% r.F. |
| Na2SO4 |
79 |
0 |
0 |
| Na2SO4+NaCl (1:1 molare Mischung) | 157 | 32 | 15 |
Kristallisationsdruck[Bearbeiten]
Bei der Kristallisation aus wäßriger Lösung läßt sich für Mirabilit ein Kristallisationsdruck von 7,2-8,3 N/mm2 angeben.
Hydratationsverhalten[Bearbeiten]
siehe Natriumsulfat
Analytischer Nachweis[Bearbeiten]
Mikroskopie
[Bearbeiten]
Laboruntersuchung:
Durch mikroskopische Beobachtungen des Lösungsverhaltens sind die gute Wasserlöslichkeit und Ethanolunlöslichkeit zu verifizieren. Thenardit und Mirabilit besitzen keine morphologische Charakterisitka, die bei einfachen Rekristallisationsversuchen zur Identifizierung beitragen können. Vielmehr ist eine große Bandbreite unterschiedlichster Erscheinungsformen beobachtbar.
Brechungsindizes: nx = 1,395; ny =1,396-1,410; nz =1,398-1,419
Doppelbrechung: Δ = 0.04-0,023
Kristallklasse: monoklin
Polarisationsmikroskopische Untersuchung:
In Abhängigkeit von den vorliegenden Luftfeuchte- und Temperaturbedingungen verändern Kristalle des Rohprobematerials und des rekristallisierten Präparates ihren Kristallwassergehalt. An trockner Luft (mit r.F. < 80% und Raumtemperatur) verliert Mirabilit sein Kristallwasser und geht in Thenardit über. Dieser Vorgang kann mikroskopisch klar nachvollzogen werden, wenn der Prozeß der Rekristallisation beobachtet wird. Mirabilit weist charakteristische anormale Interferenzfarbe auf, im Zuge des Wasserverlustes und Entstehen von Thenardit schwächen sich die anormalen Interferenzphänomene zunehmend ab.
Verwechslungsmöglichkeiten:
Generell ist die Unterscheidung einer bestimmten Anzahl von Sulfaten (die unten aufgelistet sind und wozu Thenardit zählt) ohne mikrochemische Bestimmung der Anionen problematisch, da die Brechungsindizes der Salze dicht beieinander liegen, und alle Salze eine niedrige Doppelbrechung aufweisen. Hilfreich ist die Verwendung eines Immersionsmittels mit einem nD-Wert von 1,48. Eine Differenzierung innerhalb dieser Gruppe wird damit möglich. Außerdem können die unten genannten Eigenschaften als Abgrenzungskriterien hinzugezogen werden.
Eindeutig bestimmbar wird Thenardit durch die Möglichkeit, nach Auflösung des Probematerials im Zuge der Rekristallisation das Phänomen anormaler Interferezfarben beobachten zu können, sprich Mirabilit in der hohen Hydratstufe zu identifizieren, und somit indirekt Thenardit nachzuweisen.
| Salzphase | Unterscheidungsmerkmale zu Thenardit und Mirabilit |
| Boussingaultit, (NH4)2Mg(SO)4 • 6H20 | keine anormalen Interferenzfarben / schiefe Auslöschung |
| Pikromerit, K2Mg(SO4)2 • 6H20 | keine anormalen Interferenzfarben / schiefe Auslöschung |
| Bloedit, Na2Mg(SO4)2 • 6H20 | alle Indizes >1,48 / keine anormalen Interferenzfarben / schiefe Auslöschung / optisch negativ orientiert. |
| Glaserit, K3Na(SO4)2 | alle Indizes >1,48 / keine anormalen Interferenzfarben/schiefe Auslöschung |
| Arkanit, K2SO4 | alle Indizes >1,48 / keine anormalen Interferenzfarben |
| Magnesiumformiat, Mg(HCO2)2 • 2H2O | vergleichsweise hohe Doppelbrechung / keine anormalen Interfernzfarben / schiefe Auslöschung |
Betrachtung von Mischsystemen:
Mischsystem Na+– Ca2+– SO4 2-: Der Ausfall von Gips erfolgt im Zuge der Rekristallisation entsprechend der geringeren Löslichkeit desselben zuerst. Der charakteristische nadelige Habitus von einzelnen Gipskristallen wie auch von Aggregaten bleibt bestehen. Der Ausfall von Natriumsulfat erfolgt später, das eigentliche Kristallwachstum vollzieht sich merklich schneller. Die Morphologie ist unspezifisch.
Mischsystem Na+– SO4 2-– Cl-: Der Ausfall der beiden Partikelsorten beginnt etwa zeitgleich. Halit mit charakteristischer Morphologie, Natriumsulfat in extrem variierender Gestalt.
Salze und Salzschäden im Bild[Bearbeiten]
Am Objekt[Bearbeiten]
Unter dem Polarisationsmikrokop[Bearbeiten]
- Natriumsulfatktistakkisation/Mirabilit ziwschen zwei Objektträgern
Unter dem Rasterelektronenmikroskop[Bearbeiten]
Weblinks
[Bearbeiten]
- ↑ http://webmineral.com/data/Mirabilite.shtml gesehen 29.07.2010
- ↑ http://www.mindat.org/min-2725.html gesehen 29.07.2010
- ↑ http://www.mineralienatlas.de/lexikon/index.php/MineralData?mineral=Mirabilit gesehen 29.07.2010
Literatur[Bearbeiten]
[Filter fehlt]

